TARGET DISEASE 対象疾患
神経膠腫(グリオーマ)
概要
脳は神経細胞と神経膠細胞(グリア細胞)から構成されていますが、神経膠腫(グリオーマ)は、脳内の神経膠細胞由来と考えられています。原発性中枢神経系(脳・脊髄)腫瘍のうち25〜27%を占め、2番目に多い腫瘍です。腫瘍の組織学的特長と遺伝子異常から、星細胞系腫瘍(せいさいぼうけいしゅよう:astrocytic tumor)、乏突起膠細胞系腫瘍(ぼうとっきこうさいぼうけいしゅよう:oligodendroglial tumor)、上衣系腫瘍(じょういけいしゅよう:ependymal tumor)に大別され、さらに悪性度がグレード 1(軽度)からグレード 4(高度)に分類されます。脳実質内に発生し浸潤性に増殖することを特長とし、しばしば低悪性度の腫瘍が経過中に高悪性度に転化することが知られています。
近年、腫瘍の遺伝子異常(IDH遺伝子の変異の有無、1p/19q共欠失1)の有無、MGMT遺伝子の
メチル化の有無など)が、神経膠腫の中での腫瘍型分類、化学療法反応性予測、予後予測に重要であることが示されています。
1)(腫瘍の)染色体1番の短腕と19番長腕の欠失。1p/19q共欠失をもつ神経膠腫は、化学療法反応性が比較的高いことが知られています。当院では、神経膠腫の治療法選択や予後予測に重要な遺伝子異常の検査を、先進医療として行っています。
原因・症状
神経膠腫は、腫瘍発生起源となる神経膠細胞あるいはその前駆細胞に、遺伝子異常が蓄積して発生すると考えられています。稀に遺伝的な素因が関係している例もありますが(遺伝性腫瘍症候群)、DNA複製エラー(自然突然変異)が主因であり、遺伝的素因や環境因子の関与は少ないと考えられています。
症状には、巣症状と頭蓋内圧(脳圧)亢進症状があります。巣症状は,腫瘍の発生部位に関係して生じる、麻痺、失語、視野障害、脳神経症状などです。例えば、腫瘍が運動野や運動線維に影響を及ぼせば、反対側の手足に脱力(麻痺)が生じますし、言語中枢のある左前頭葉や左側頭葉の腫瘍では、言葉が出しにくい、相手の言うことが理解できない、などの失語症状が生じます。特に左前頭葉の腫瘍では、しばしば口数が少なくなり、うつ症状に似ていることもあります。てんかん発作も、頻度の高い症状の一つです。頭蓋内圧亢進症状は、腫瘍の発生部位によらず、腫瘍およびその周囲浮腫などにより、頭蓋骨で囲まれた閉鎖空間の圧が上昇することによる症状です。
頭痛、吐き気、嘔吐、視力低下(うっ血乳頭)などであります。進行すると脳ヘルニアをきたし,意識が低下し、生命にかかわります。小脳に発生した腫瘍などにより、髄液の循環経路である脳室の狭窄や閉塞が生じれば、水頭症による急性の頭蓋内圧亢進をきたすことがあります。
検査・診断
診断の主要な手段はMRIなどの画像診断です。CTは出血や石灰化の確認に有用です。神経膠腫は一般に、MRI T1強調画像で低信号(黒く)、T2強調画像やFLAIR画像で高信号(白く)で描出されます。grade 3, 4などの悪性神経膠腫では、造影剤による増強効果を示すことが多く、しばしば周囲に広範な浮腫を伴います。MRIやCTでの画像所見、発生部位、年齢、症状経過(いつ頃からどのような症状があったか)などから、脳腫瘍であるか、神経膠腫であるか、神経膠腫の中でどのタイプか、グレードは?、摘出手術が必要か、緊急性は?、などを判断します。
摘出手術が必要と考えられた場合は、さらに、CT血管造影検査、メチオニンPET2)、神経線維のトラクトグラフィー3)、機能的MRI4)、和田テスト5)などの精査を行い、手術のリスク、手術戦略を詳細に検討します。
2)保険適用外
3)当院では、MRI画像の上に、神経線維の走行を重ね合わせたfusion画像により、腫瘍と神経線維の関係を詳細に検討しています。
4)functional MRI。言語優位半球(右と左のどちらに言語中枢があるか)や運動野の場所の確認に有用です。
5)プロポフォールテストとも呼ばれます。言語優位半球の確認に重要な検査です。
治療法
ほとんどの神経膠腫は脳内を浸潤性(しみこむように)に発育する腫瘍ですが、脳という臓器特殊性(広く切除することができない)ゆえに、一般に、手術による根治切除は困難とされています。一方,神経膠腫においては、組織型、 グレードを問わず、手術摘出率や残存腫瘍体積が患者さんの生命予後と関係するとされています。そのため、術前画像から神経膠腫が予想される場合には、術中神経モニタリング,手術ナビゲーションシステム,光線力学的診断6),覚醒下手術7)などの手術支援技術を駆使して、最小限の手術合併症で最大限の摘出をする努力がなされます。深部腫瘍や脳幹腫瘍など、摘出困難な部位に発生した腫瘍、あるいは高齢患者などに対しては、生検術に留めることもあります。
手術後、摘出された腫瘍の組織型やグレードに応じて、放射線治療や薬物治療の必要性、範囲、量などが検討されます(参考論文1)。
代表的な神経膠腫である膠芽腫に対する標準治療は、可及的腫瘍摘出後の放射線・テモゾロミド8)併用療法です。そのほか、交流電場治療システム(オプチューン®︎)9)、ベバシズマブ(アバスチン®︎)10)などの併用が検討されます(脳腫瘍診療ガイドラインhttps://www.jsn-o.com/guideline/index.html)。
6)腫瘍親和性かつ光感受性(腫瘍に選択的に蓄積し、かつ蛍光を発する)の試薬(5-アミノレブリン酸(アラベル®︎))を利用して、手術中に腫瘍の存在部位を蛍光診断する技術です。
7)手術中に患者さんに起きて頂き、言葉や手足の動きを実際に観察しながら行う手術です。言語野や運動野に近い腫瘍の摘出の際に行われます。当院は、覚醒下手術認定施設です。
8)アルキル化剤という種類の抗がん剤(錠剤)です。
9)低振幅の交流電場により細胞分裂の傷害を生じ抗腫瘍作用を発揮するものです。
10)VEGF(血管内皮増殖因子)を標的とする抗体で、分子標的治療薬です。
治療後経過
初期治療(手術、放射線、薬物による一連の治療)が終了した後は、組織型やグレードに応じて、経過観察が行われます(2ヶ月〜半年に1回程度のMRI検査)。手術による根治切除が困難な例が多く、また放射線や化学療法の効果も限定的であり、しばしば再発が認められます。そのため、膠芽腫をはじめ、いまだに根治の難しい例が多い状況ですが(表1)、治療法の進歩は目覚ましく、当院では様々な取り組みにより、個々の患者さんに最善の治療を提供すべく努力しています。
表1 全国脳腫瘍統計 5年生存率(参考文献2-4)
(注:遺伝子異常による分類ではなく、組織診断に基づく分類)
|
病理診断 |
5年生存率(1997-2000に手術が行われた患者) |
5年生存率(2001-04) |
5年生存率(2005-08) |
|
びまん性星細胞腫 |
68.3% |
80% |
77.1% |
|
乏突起膠腫 |
87.8% |
90.5%(乏突起膠腫、乏突起星細胞腫のデータ) |
92.5% |
|
退形成性星細胞腫 |
33.9% |
42.4% |
43.2% |
|
退形成性乏突起膠腫 |
63% |
68.3%(退形成性乏突起膠腫、退形成性乏突起星細胞腫のデータ) |
62.6% |
|
膠芽腫 |
6.9% |
10.2% |
16.0% |
実績
1990年から2011年の間に、当院で手術が行われた膠芽腫の患者さんの経過のまとめでは(参考文献5)、5年以上生存された方が10%、3年以上生存された方が24%でした。次に示すような様々な取り組みにより、近年ではさらに良好な治療成績が得られています。
慶應脳外科としての取り組み(特長)
1. 手術ナビゲーションシステムを利用した精密手術
MRI、神経線維のトラクトグラフィー、メチオニンPET画像、CT血管造影画像などに基づいた詳細な摘出プラニング、手術ナビゲーションシステムを利用した正確なフェンスポストの挿入11)、正確なマイクロサージェリー技術などにより、精密、正確な切除を目指しています(図1)。
11)境界不明瞭な腫瘍の摘出に際して、手術の最初に摘出範囲を囲うように「杭」を挿入します。
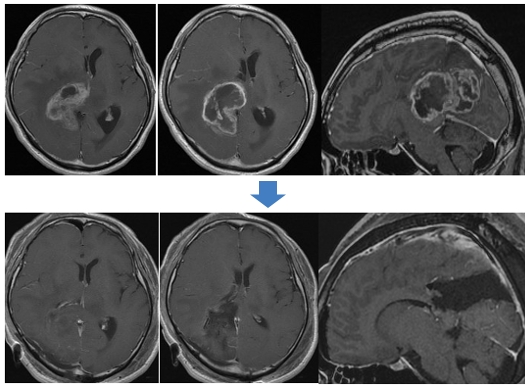
図1:巨大膠芽腫摘出例
2. 当院では覚醒下手術7)の経験が豊富であり、運動神経誘発電位(MEP)、体性感覚誘発電位(SEP)などの術中神経モニタリングと組み合わせ、最小限の手術合併症で最大限の摘出をする努力をしています。
3. 当院では、腫瘍局所療法12)として、光線力学的療法(PDT)を行なっています(下記に詳細を示します)。 術前画像に基づく腫瘍の性質の予測などから、光線力学的療法、光線力学的診断、抗がん剤脳内留置(ギリアデル®︎)を、患者さんに応じて適切に選択し、治療しています。
12)腫瘍を摘出した後に、周囲に残存している腫瘍細胞に対して行う治療。手術中に行うものとして、光線力学的療法と抗がん剤脳内留置あります。
4. 分子診断に基づく個別化治療
当院では先進医療として、神経膠腫の遺伝子異常、分子マーカーを検査しており、それらのデータに基づく、適切な個別化治療を行なっています(参考文献1)。
5. 腫瘍の化学療法反応性の予測、そして化学療法反応性を最大限に活用しての治療戦略
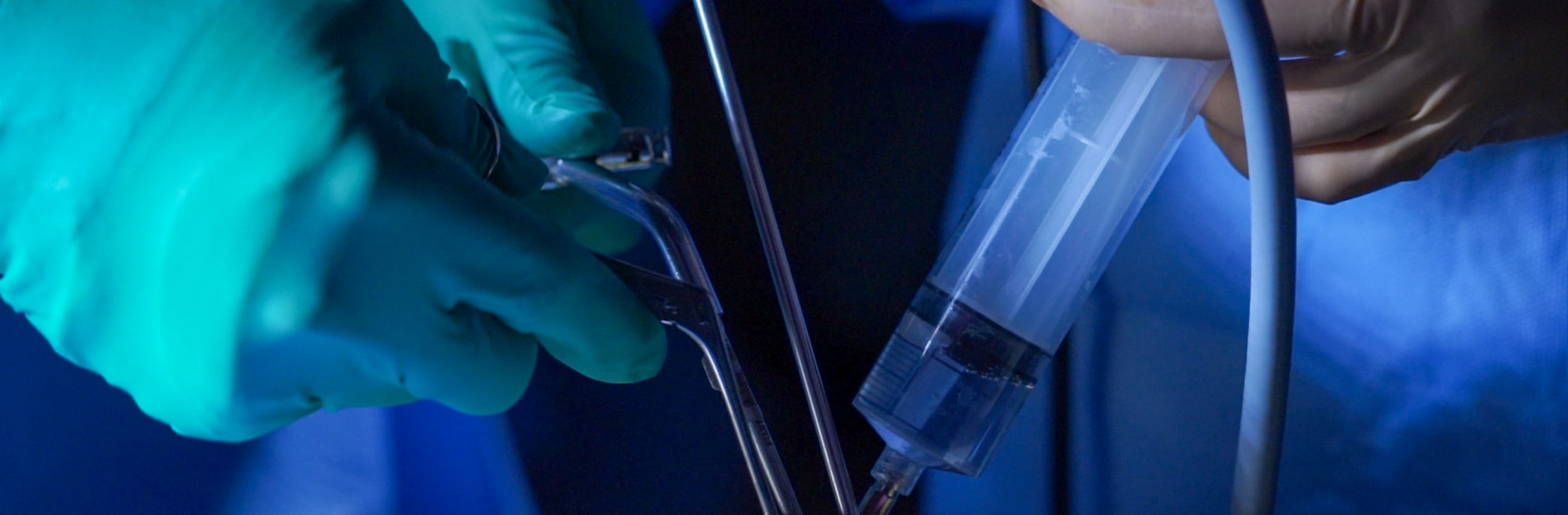
一般に神経膠腫においては、手術における腫瘍摘出率が高いほど、患者さんの生命予後が良いとされていますが(脳腫瘍診療ガイドラインhttps://www.jsn-o.com/guideline/index.html)、一方で、脳ほど機能温存が重要な臓器はありません。当院では、1p/19q共欠失1)やMGMT遺伝子のメチル化などにより、腫瘍の化学療法反応性が予測される場合は、化学療法で腫瘍が縮小した後に切除することにより、機能温存と生命予後の改善を図っています(図2)。最近では、術前の画像から、神経膠腫の組織型や遺伝子異常を予測することにより(参考文献6)、手術摘出戦略、全体の治療戦略を、手術の前に立案することにより、良好な結果が得られています。

図2:運動野そのものに発生した神経膠腫の治療例。A-C:化学療法前。E-G:化学療法後。
I-K:全摘出。最初に生検術を行い、1p/19q共欠失が確認されたため、化学療法で縮小させ、上肢の運動野から腫瘍を後退させた後に覚醒下で全摘出が行われた(10年以上、合併症、再発なく経過)(参考文献1より引用)。
6. ゲノム医療
当院は、ゲノム医療中核拠点病院です。標準治療後の万一の再発に備えて、保険診療のがん遺伝子パネル検査を積極的に行い、できる限りの治療選択肢を準備することを意識しています。
7. 看護部との密接な連携
看護部と密接に連携し、個々の患者さんに寄り添った診療を心がけています。
交流電場治療システム(オプチューン®︎)9)は、膠芽腫に対する有効な新規治療法ですが、しばしば長期の継続が難しいとされています。当院では、すでに2年以上再発なく継続されている患者さんが複数おり、看護部との連携の成果と考えています。8.ワクチン療法
患者さん(腫瘍)に応じて、ワクチン療法を検討させて頂いています。
参考論文
1) Sasaki H and Yoshida K. Treatment recommendations for adult patients with diffuse gliomas of grade II and III according to the new WHO classification in 2016.
Neurol Med Chir (Tokyo) 57: 658-66, 2017
2) The Committee of Brain Tumor Registry of Japan : Report of Brain Tumor Registry of Japan (1984-2000),Neurol Med Chir (Tokyo) 49(Suppl:PS1-96), 2009
3) The Committee of Brain Tumor Registry of Japan : Report of Brain Tumor Registry of Japan (2001-2004),13th Ed., Neurol Med Chir (Tokyo) 54(Suppl 1), 2014
4) The Committee of Brain Tumor Registry of Japan : Report of Brain Tumor Registry of Japan (2005-2008),14th Ed., Neurol Med Chir (Tokyo) 57(Suppl 1), 2017
5) Nakagawa Y et al. Clinical and molecular prognostic factors for long-term survival of patients with glioblastomas in a single-institutional consecutive cohort.
World Neurosurg. 16:165-73, 2017
6) Kanazawa et al. Imaging scoring systems for preoperative molecular diagnoses of lower grade gliomas. Neurosurg Rev. 42:433-41, 2019
光線力学的療法(Photodynamic Therapy: PDT)について
慶應義塾大学病院では、悪性神経膠腫などの原発性悪性脳腫瘍に対して、PDTによる治療を行っています。
【概要】
神経膠腫に代表される原発性脳腫瘍の多くは、周囲の脳組織に浸み込むように発育する浸潤性腫瘍です。脳腫瘍の治療においては、手術で最大限の摘出を行うことが重要ですが、脳機能を温存するために、摘出腔周囲には浸潤腫瘍細胞が残存することが少なくありません。これらの残存腫瘍細胞は、再発の原因となります。
PDTは、このような摘出腔周囲や摘出困難な部位に残存する腫瘍細胞を、可能な限り正常な細胞を傷つけることなく、選択的に治療する方法です。
この治療は、術中に開頭した状態で、腫瘍の摘出後に連続して行い、腫瘍の残存が疑われる部位に対し、レーザー光を照射することにより行われます。
PDTは、早期肺癌、遺残再発食道癌にも使用されますが、原発性悪性脳腫瘍に対しては、2013年9月に薬事承認、2014年1月に保険収載されました。
【作用機序】
PDTでは、腫瘍に選択的に蓄積する光感受性物質である、タラポルフィンナトリウム(レザフィリン®)を使用します。手術の前日にレザフィリンを患者さんに投与し、手術中(腫瘍摘出後)にレーザー光を照射することで、レザフィリンが蓄積した腫瘍細胞で光化学反応が惹起されます。この化学反応により発生した一重項酸素(ROS:reactive oxygen species)の強い酸化作用で細胞が選択的に変性・壊死します。
【注意点(遮光管理)】
光線過敏症などの副作用の可能性があるため、投与から約2週間は、500ルクス以下の環境を保持する目的で遮光管理が必要となります。具体的には、サングラスや帽子などを着用して頂き、目などの粘膜や皮膚に強い光が当たらないように生活をして頂きます。約2週間経過した時点で、光線過敏試験を施行し、問題がなければ遮光管理を解除し、日常生活に戻って頂きます。
受診をご希望の患者さんへ
外来受診については、慶應義塾大学病院のホームページ内の「初めて受診する方」に詳細をお示ししておりますが、「予約制」「紹介制」をとらせていただいています。
- 一人一人の患者さんを十分に診察、説明させていただきたく、またお待ちいただく時間を短縮するために、外来は予約制とさせていただいております。
- 予約の際には、ご病状を速やかに把握させていただくため、現在かかりつけの医療機関からの紹介状をお持ちいただくようお願い申し上げます(紹介制)。これまでに受けた検査(MRIやCTなどの画像検査、採血検査など)の結果もお持ちいただけますとたいへん助かります。
- お手数をおかけいたしますが、かかりつけの医療機関から、下記の予約方法で本疾患担当医師の外来を予約していただきたく存じます。
<脳神経外科外来の予約方法>
外来予約窓口:(電話)03-3353-1257 にお電話ください。
※外来予約窓口 受付時間:月~金曜日 8:30~19:00
(土曜日は17:00までの受付となります)
患者さんをご紹介される医療機関のみなさまへ
当院ホームページにご紹介に関する詳細をご説明しています。
こちらよりご確認ください。